Santé sexuelle, complétez vos consultations médicales, en vidéo
Doctical apporte une réponse innovante au manque de temps médical, et à la difficulté de parler de santé intime en consultation, particulièrement dans un parcours de soins contre le cancer.
Accéder à mon espace

+2000
patients en 2 ans
95%
sont satisfaits des vidéos (enquête ANAMACAP)
96%
sont satisfaits des ateliers en visio
Sur Doctical, 1 question = 1 réponse médicale en vidéo
Des médecins experts vous expliquent, en quelques minutes, toutes les solutions qui s’offrent à vous.
Accès gratuit. Inscrivez-vous et consultez les vidéos librement, 24h/24, 7 jours/7
Des informations pratiques, chez vous, à votre rythme
Accès abonné : posez vos questions à nos médecins, participez à des ateliers en visio et optez pour plus d'informations pour un accompagnement plus personnalisé.
Je consulte
Dysfonction érectile
Sécheresse vaginale
Cliquez sur le programme de votre choix.
Améliorer l'érection en cas de cancer de prostate
0 video
Je m'inscris au prochain atelier visio "Vacuum et anneaux péniens"
Jeudi 2 Mai 2024 à 18h
5 vidéos
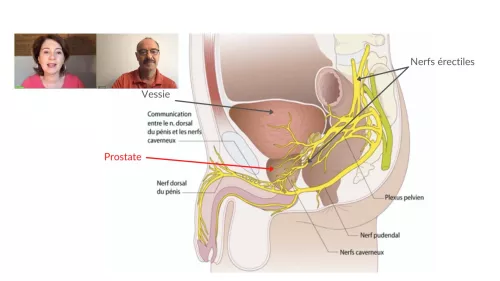
Prostatectomie radicale , quelles conséquences pour l'érection ?
Programme vidéo avec le Dr Catherine Solano, médecin sexologue et andrologue à l'hôpital Cochin de Paris, auteur de « la mécanique sexuelle de l’érection » et « les trois cerveaux sexuels » aux éditions Robert Laffont.
8 vidéos
Viagra®, Cialis®... comment utiliser au mieux les médicaments en comprimés après une prostatectomie ?
Programme vidéo avec le Dr Catherine Solano, médecin sexologue et andrologue à l'hôpital Cochin de Paris, auteur de « la mécanique sexuelle de l’érection » et « les trois cerveaux sexuels » aux éditions Robert Laffont.
8 vidéos
Comment utiliser Vitaros® pour l'érection
Programme vidéo avec le Dr Pierre Desvaux, médecin sexologue et andrologue

19 vidéos
Edex® et Caverject®, les injections pour l'érection, mode d'emploi
Programme vidéo avec le Dr Pierre Desvaux, médecin sexologue et andrologue, un expert des injections intra caverneuses.

11 vidéos
Vacuum et anneau pénien
Programme vidéo avec le Dr Catherine Solano, médecin sexologue et andrologue à l'hôpital Cochin de Paris, auteur de « la mécanique sexuelle de l’érection » et « les trois cerveaux sexuels » aux éditions Robert Laffont.

66 vidéos
Tout sur l'implant pénien
Programme vidéo animé par le Pr Frédéric Staerman, chirurgien urologue, professeur d’urologie, à l’origine à l’origine des diplômes de chirurgie de la verge, d’uro-oncologie et de sexologie de l’Est. Il consulte à la clinique Bezannes à Reims.

36 vidéos
Médicaments en comprimés pour l'érection
Programme vidéo avec le Dr Catherine Solano, médecin sexologue et andrologue à l'hôpital Cochin de Paris, auteur des livres « La mécanique sexuelle de l’érection » et « Les trois cerveaux sexuels » aux éditions Robert Laffont.
Je consulte les vidéos gratuites maintenant
" Les vidéos sont simples et riches et on les comprend facilement. Cet accompagnement est indispensable pour garder le moral car seul on ne sait pas tout et on a besoin de conseils et d'échanges pour s'adapter à une nouvelle vie sexuelle." Témoignage de Patrick, 06/2022.
Informez-vous librement, à votre rythme et en confiance avec nos experts

Dr. Pierre Bondil
Chirurgien urologue oncologue sexologue, Président du Comité scientifique

Pr. Frédéric Staerman
Chirurgien urologue, professeur d’urologie

Dr Pierre Desvaux
Médecin sexologue et andrologue, expert des injections intra caverneuses

Dr. Catherine Solano
Médecin sexologue, andrologue
Nos patients témoignent
Patrick
26/02/2024
Bravo pour cette belle formule et pour le choix des interventions. Un enseignement précieux et indispensable pour toutes personnes concernées par le sujet.
Alain
26/02/2024
Excellent, pertinence des interventions et de la présentation .Grand intérêt de la présentation médecin/patient
Dominique
25/02/2024
Pédagogique, documenté, clair, incitatif, souriant
Jean
24/02/2024
SATISFAISANT DANS LA MESURE OU J'AI DES REPONSES A MES INTERROGATIONS
Franck
23/02/20224
Exposé clair et honnête et bonne partie dédiée aux questions.
Michel
23/02/2024
C’est très bien. Un grand merci à vous.
Marc
21/02/2024
Atelier bien animé qui reste centré jusqu à la fin sur les patients
Patrick
10/2023
Excellent atelier, permettant d'aborder ces problèmes d'érection, très intimes et délicats à exprimer, dans une atmosphère positive et chaleureuse. Le cadre médical apporte un haut niveau de confiance envers les solutions exposées, par comparaison aux forums disponibles sur les réseaux sociaux. Avis publié.
Jacques
07/2023
Un grand merci au site doctical d'exister et en particulier aux Dr Solano et Desvaux. Je viens de voir les vidéos sur vitaros et edex. Elles sont très bien faites. J'ai été opéré d'une prostatectomie radicale fin mai 2023. Je viens de commencer l'edex car vitaros n'a donné aucun effet.
Abdou
06/2023
Merci beaucoup Docteur. Je vais continuer de suivre vos conseils qui m'ont été d'une grande aide. Je me sens plus épanoui aujourd'hui dans mon quotidien, dans mon boulot et dans mes relations. Ce problème m'avait psychologiquement affecté et aujourd'hui je baigne dans un bien être profond et tout ça grâce à vous. J'ai consulté beaucoup de spécialistes, dépensé beaucoup sans jamais trouver de solution et vous avez réussi à me mettre sur la bonne voie. Je vous en suis profondément reconnaissant. Heureusement qu'on a des personnes comme vous dans la société. Bien à vous !
Jacques
07/2023
Beaucoup d'informations pertinentes exprimées dans un vocabulaire simple pour des patients qui n'ont pas de formation médicale.Avis publié.
Claude
06/2023
J'ai été particulièrement intéressé par le thème de cet atelier (ndlr. "la sexualité avec érection difficile ou sans érection") qui me concerne à 100 % . Je me rends compte que n'ayant pas eu les bonnes informations après mon prostatectomie , je n'ai pas pu bénéficier des conseil et d'un traitement approprié à ma situation .
Kamal
05/2023
Je vous remercie pour l’organisation de cette Visio à laquelle j’ai assisté. Cette visio a té très importante pour moi. Elle ml’a permis de me remobiliser et de me sentir moins seul. J’ai beaucoup aimé vos interventions et la manière dont vous parlé de cette maladie. Encore merci à vous.
Bernard
04/2023
Merci d'avoir organisé cet atelier qui était très clair et qui m'a apporté une bonne rétrospective en tant qu' "ancien opéré " ( depuis plus de 3 ans ). Merci plus particulièrement à vous , Dr Solano , pour avoir apporté la touche féminine qui me semble indispensable sur un tel sujet.
Bruno
02/2023
Merci à vous trois pour cette heure passée avec vous. Il est évident que vous faites partie des membres du corps médical pour lesquels les effets négatifs de la prostatectomie et de la radiothérapie pelvienne ne sont pas secondaires mais bien des indésirables. Pour ma part l'anti-hormonothérapie a été très dangereuse. Avec tous ses effets j'allais droit au suicide (dormir 2h par nuit n'est pas secondaire) et je l'ai abandonnée à la deuxième injection trimestrielle. (...) Dommage que je n'aie pas eu vos conseils fin 2015, je ne serais peut-être pas dans l'état actuel.
P.
06/2022
Les vidéos sont simples et riches et on les comprend facilement. cet accompagnement est indispensable pour garder le moral car seul on ne sait pas tout et on a besoin de conseils et d'échanges pour s'adapter à une nouvelle vie sexuelle.
L.
05/22
Très intéressant. Le problème du dysfonctionnement érectile a été abordé par mon urologue avant et après l'intervention, mais il n'y a pas de suivi. Le sujet est abordé en fonction de la pudeur de l'urologue. Il m'a recommandé de regarder sur Youtube le mode d'emploi de Vitaros, ce qui m'a conduit à deux épisodes de priapismes très pénibles.
Ce programme vidéo vous explique ce qu’il faut savoir sur la sécheresse intime en cas de cancer, et quelles solutions s'offrent à vous.
Surmonter la sécheresse vaginale en cas de cancer

42 vidéos
Sécheresse intime, ce qu'il faut savoir
Programme vidéo avec le Dr Marion Aupomerol, gynécologue sexologue à Gustave Roussy.
24 vidéos
Traitements hormonaux de la sécheresse vulvo-vaginale
Programme vidéo avec le Dr Marion Aupomerol, gynécologue sexologue à Gustave Roussy.
11 vidéos
Traitements sans hormones de la sécheresse vulvo-vaginale
Programme vidéo avec le Dr Catherine Solano, médecin sexologue à l'hôpital Cochin de Paris, auteur de « les trois cerveaux sexuels » aux éditions Robert Laffont.
Je consulte les vidéos gratuites maintenant
" Les vidéos sont simples et riches et on les comprend facilement. Cet accompagnement est indispensable pour garder le moral car seul on ne sait pas tout et on a besoin de conseils et d'échanges pour s'adapter à une nouvelle vie sexuelle." Témoignage de Patrick, 06/2022.
Informez-vous librement, à votre rythme et en confiance avec nos experts

Dr. Marion Aupomerol
Gynécologue médicale et sexologue

Dr. Catherine Solano
Médecin sexologue, andrologue
Nos patients témoignent
Mel
08/2023
Je pense que ces types de formations devraient être préalables à un rendez-vous avec un spécialiste et permettraient une consultation pour celles et ceux qui n'oseraient pas ou qui croiraient qu'il n'y a rien à faire.
Michèle
04/2023
Je viens de découvrir votre site. Merci d’exister! Je dois décider d’une intervention chirurgicale, ou y renoncer, après une mastectomie réalisée en juin 2001. J’ai beaucoup de difficulté à accepter mon corps comme il est maintenant. J’ai 76 ans. Alors, inutile, me direz-vous? Je ne sais pas qui ou quoi peut éclairer ma réflexion.
J.
08/2022
Ces vidéos sont très intéressantes, le classement par thèmes est organisé, le contenu est accessible à tous sans avoir besoin de connaissance médicales. BRAVO